Im Projekt „Gentherapie der Lunge in vitro – den Einsatz transgener Tiere auf ein Minimum reduzieren“ wurde mit humanen Systemen erforscht, wie sich eine Gentherapie der menschlichen Lunge in vitro nachstellen lässt, um den Einsatz von Tierversuchen in diesem schnell wachsenden Forschungsbereich zu reduzieren.
Dazu wurden unterschiedliche Mechanismen wie die Partikeldeposition, die Aufnahme in die unterschiedlichen Lungenzellen und die Wirksamkeit nachgeahmt. Hierfür wurden neben Zelllinien auch primäre Alveolarzellen der menschlichen Lunge eingesetzt. Eine große Bedeutung kam dabei der primären autologen Kokultur der unteren Atemwege zur Untersuchung neuer pulmonaler Formulierungen zu.
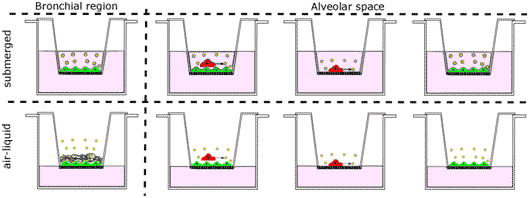
Zur Deposition der Partikel auf den Zellen wurden spezielle Instrumente wie das „Vitro Cell Cloud System“ eingesetzt. Dieses erlaubt es, neue Medikamente unter sogenannten „air-liquid“-Bedingungen direkt auf die Zellen zu deponieren. Die Zellen befinden sich dabei in direktem Kontakt zur Umgebung, was eine gute Simulation der in vivo-Situation ermöglicht.
Im Versuchsaufbau wurden die oberen Atemwege durch die Zelllinie Calu-3 nachgeahmt, die unteren Atemwege wurden durch primäre alveolare Lungenzellen und Kokulturen nachgestellt. So wurde untersucht, welchen Einfluss Makrophagen in den unteren Atemwegen oder Mucus aus den oberen Atemwegen auf die Wirksamkeit neuer Therapieformen haben.

 Deutsch
Deutsch